Catalyseurs à base de métaux précieux : L'amplificateur de performance - Le support
Chapitre 1 : Introduction
Un catalyseur à base de métaux précieux est un matériau qui peut modifier la vitesse d'une réaction chimique sans être lui-même consommé dans les produits finaux. Bien que presque tous les métaux précieux puissent servir de catalyseurs, les plus couramment utilisés sont le platine, le palladium, le rhodium, l'argent et le ruthénium, le platine et le rhodium ayant les applications les plus étendues. Leurs orbitales d'électrons d partiellement remplies adsorbent facilement les réactifs sur la surface avec une force de liaison modérée, facilitant la formation de "composés actifs" intermédiaires et conférant ainsi une activité catalytique élevée. Associés à des propriétés supérieures telles que la résistance aux températures élevées, à l'oxydation et à la corrosion, ils sont devenus l'un des matériaux catalytiques les plus importants.
Les catalyseurs à base de métaux précieux sont indispensables dans de nombreux domaines clés en raison de leur activité catalytique et de leur sélectivité exceptionnelles. Dans le domaine de l'assainissement de l'environnement, ils sont largement utilisés dans les systèmes de purification des gaz d'échappement des automobiles et dans les processus de combustion industrielle pour convertir efficacement les polluants toxiques tels que le monoxyde de carbone, les oxydes d'azote et les composés organiques volatils en gaz inoffensifs, réduisant ainsi de manière significative les émissions. Ils jouent également un rôle essentiel dans d'autres domaines de la protection de l'environnement, tels que la purification de l'air et le traitement des eaux usées. Dans la production industrielle, ils jouent un rôle central dans la synthèse chimique, en améliorant les taux de réaction et la sélectivité des produits grâce à des réactions catalysées telles que l'hydrogénation, l'oxydation et la carbonylation. En outre, dans le secteur de pointe de l'énergie, les catalyseurs à base de métaux précieux sont la pierre angulaire des technologies de l'énergie hydrogène, faisant partie intégrante de la production d'hydrogène, du fonctionnement des piles à combustible et du stockage de l'hydrogène, faisant ainsi progresser la conversion et l'utilisation de l'énergie propre.
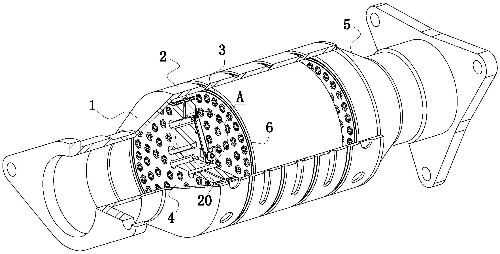
Fig. 1 Diagramme structurel du convertisseur catalytique à trois voies de l'automobile
Toutefois, les inconvénients inhérents aux métaux précieux - leur rareté à l'échelle mondiale, leur coût élevé et leur susceptibilité à la désactivation par frittage, lixiviation et empoisonnement - limitent considérablement leur application commerciale à grande échelle. La clé pour relever ces défis ne réside pas dans les métaux précieux eux-mêmes, mais dans leur "fondation" - le support. La science catalytique moderne révèle que le support est loin d'être un échafaudage physique inerte ; il s'agit d'une plate-forme multifonctionnelle et d'un partenaire synergique essentiel pour surmonter les limites des métaux précieux. Sa valeur fondamentale se manifeste dans deux aspects clés :
Le support, avec sa surface spécifique élevée et ses nombreux défauts de surface, fournit des "sites d'ancrage" sûrs pour les nanoparticules de métaux précieux ou même les atomes uniques, permettant une dispersion au niveau atomique. Cela permet non seulement de maximiser l'exposition des sites actifs, ce qui améliore considérablement l'efficacité de l'utilisation des atomes, mais aussi d'empêcher efficacement la migration et l'agglomération (frittage) des particules à haute température grâce à des contraintes spatiales physiques et à de fortes interactions, ce qui améliore fondamentalement la stabilité du catalyseur.
Des interactions profondes existent entre le support et le métal précieux. Grâce à des effets électroniques (par exemple, les interactions fortes métal-support, SMSI), le support peut moduler la densité du nuage électronique du métal précieux, optimisant ainsi sa force d'adsorption pour les réactifs, ce qui améliore l'activité catalytique intrinsèque et la sélectivité. En outre, l'acidité/basicité inhérente à la surface ou les propriétés redox du support peuvent catalyser en synergie des réactions avec les sites actifs du métal précieux, permettant des voies de réaction complexes impossibles à atteindre par des composants uniques, construisant collectivement des systèmes catalytiques bifonctionnels efficaces.
Chapitre 2 : Fonctions essentielles et mécanismes du support
Dans la conception des catalyseurs à base de métaux précieux, le support n'est pas simplement un récipient de réaction passif, mais un composant clé qui joue de multiples rôles actifs. Ses mécanismes fonctionnels influencent profondément les performances finales du catalyseur, principalement dans quatre domaines :
1. Dispersion et stabilisation
La fonction première du support est d'agir comme un "ancrage" pour les nanoparticules de métaux précieux. Une surface spécifique élevée (par exemple, des centaines de m2/g) fournit de nombreux sites de chargement, ce qui permet au métal précieux d'être fortement dispersé à l'échelle nanométrique ou même atomique, maximisant ainsi l'exposition des sites actifs et améliorant l'efficacité de l'utilisation atomique. Sans support, les nanoparticules de métaux précieux, en raison de leur énergie de surface élevée, migrent facilement, s'agglomèrent et se frittent à des températures élevées, ce qui entraîne une réduction drastique de la surface active et une désactivation. En outre, les structures poreuses de nombreux supports peuvent créer un effet de confinement, limitant les particules métalliques dans les nanocavités ou les couches intermédiaires - créant ainsi des "nanoréacteurs" - qui entravent physiquement leur mouvement et leur croissance, ce qui améliore encore la stabilité thermique.

Fig. 2 Matériaux poreux
2. Effets électroniques
De profondes interactions électroniques existent entre le support et le métal précieux, notamment l'interaction forte métal-support (SMSI). Si l'on prend l'exemple du système Pt/TiO2, après un traitement de réduction à haute température, une partie du Ti4+ à la surface du TiO2 est réduite et migre pour recouvrir la surface des nanoparticules de Pt, formant ainsi une couche de sous-oxyde. Ce processus s'accompagne d'un transfert d'électrons du TiO2 vers le Pt, ce qui modifie la densité du nuage d'électrons du Pt et, par conséquent, sa force et son mode d'adsorption des molécules réactives (par exemple, CO, O2). Ce "contrôle à distance" par des effets électroniques peut améliorer de manière significative l'activité catalytique et la sélectivité pour des réactions spécifiques et même conférer une résistance à l'empoisonnement.
3. Catalyse synergique
De nombreux supports ne sont pas inertes ; leurs surfaces possèdent des sites acides/basiques ou des sites catalytiques actifs inhérents, permettant une catalyse synergique avec le métal précieux, constituant ainsi un mécanisme "bifonctionnel". Par exemple, dans le reformage catalytique du raffinage du pétrole, le Pt du catalyseur Pt/γ-Al2O3 est responsable de l'hydrogénation/déshydrogénation des oléfines, tandis que les sites acides de la surface γ-Al2O3 facilitent l'isomérisation des carbocations ; les deux fonctions agissent ensemble pour reconstruire les molécules d'hydrocarbures. Un autre exemple concerne les réactions à l'anode des piles à combustible, où les espèces RuOH dans les catalyseurs PtRu/C favorisent l'activation de l'eau, fournissant des espèces OH aux sites Pt adjacents pour oxyder le CO, ce qui résout le problème de l'empoisonnement des catalyseurs Pt par le CO.
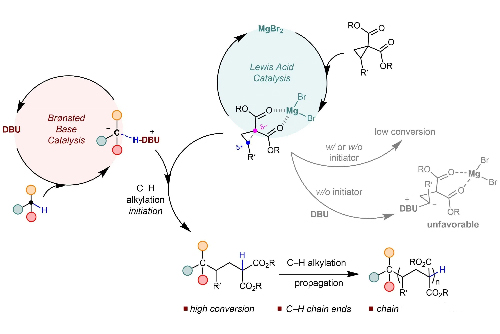
Fig. 3 Catalyse coopérative molécule organique de petite taille/métal
4. Transfert de masse et de chaleur
La structure physique du support détermine l'efficacité du transport des réactifs et des produits. Un réglage précis de la structure poreuse (y compris la taille des pores, leur volume et leur connectivité) permet d'optimiser les taux de diffusion et d'éviter les pertes d'efficacité de la réaction dues aux limitations du transfert de masse. Les macropores favorisent un transfert de masse rapide, les mésopores conviennent au chargement des nanoparticules et facilitent les réactions, et les micropores peuvent permettre une sélectivité de forme. Simultanément, d'excellents supports possèdent une stabilité thermique et une conductivité thermique élevées, ce qui leur permet de résister à des environnements de réaction exothermique à haute température, d'évacuer rapidement la chaleur de la réaction et d'empêcher l'effondrement de la structure du catalyseur et le frittage du composant actif causés par une surchauffe locale.
Chapitre 3 : Principaux types de supports pour les catalyseurs à base de métaux précieux et leurs caractéristiques
1. Supports en oxyde
Les supports oxydes constituent la catégorie la plus étudiée et la plus largement appliquée.
γ-Al2O3: Connu sous le nom de "support de travail", ses avantages comprennent une surface spécifique élevée, une acidité de surface appropriée et une bonne résistance mécanique. Ces propriétés le rendent idéal pour les catalyseurs automobiles à trois voies (chargement de Pt, Pd, Rh) et les catalyseurs d'hydrodésulfuration (chargement de Pd).
SiO2: Possède généralement une surface neutre et une surface spécifique élevée. Son inertie de surface signifie qu'il n'interfère pas avec l'activité intrinsèque du métal précieux. Le SiO2 mésoporeux accordable peut être préparé par des méthodes de templating et est largement utilisé dans les réactions d'hydrogénation et d'oxydation sélectives.
TiO2 : Outre sa surface spécifique élevée, sa caractéristique la plus importante est sa capacité à former de fortes interactions métal-support (SMSI) avec les métaux précieux, ce qui améliore considérablement les performances catalytiques. Parallèlement, TiO2 est un excellent semi-conducteur photosensible ; lorsqu'il est associé à Au, Pt, etc., il présente un grand potentiel en photocatalyse pour la séparation de l'eau et la dégradation des polluants.
CeO2 : possède une capacité unique de stockage de l'oxygène (OSC) qui lui permet de passer rapidement d'une atmosphère oxydante à une atmosphère réductrice par le biais du cycle Ce4+/Ce3+, régulant ainsi efficacement la concentration d'oxygène dans l'environnement de réaction. Cette caractéristique le rend indispensable dans la purification des gaz d'échappement des automobiles (en tant que co-catalyseur) et dans les réactions liées à l'oxydoréduction.
Tableau 1 : Comparaison des principales caractéristiques des supports d'oxyde
|
Type de support |
Surface spécifique |
Propriété de la surface |
Caractéristiques principales |
Applications typiques |
|
γ-Al2O3 |
Forte |
Faiblement acide |
Résistance mécanique élevée, bonne stabilité thermique |
Nettoyage des gaz d'échappement, hydrotraitement |
|
SiO2 |
Élevée |
Neutre |
Taille des pores réglable, surface inerte |
Hydrogénation sélective, oxydation |
|
TiO2 |
Moyen |
Amphotère |
SMSI, activité photocatalytique |
Photocatalyse, oxydation du CO |
|
CeO2 |
Moyen |
De base |
Excellente capacité de stockage de l'oxygène |
Catalyseurs à trois voies, réaction de déplacement des gaz vers l'eau |
2. Supports de matériaux en carbone
Les matériaux en carbone sont remarquables pour leur conductivité et leur diversité structurelle.
Carbone activé: Il présente une surface spécifique extrêmement élevée et d'abondants groupes fonctionnels de surface (par exemple, -OH, -COOH), ce qui le rend facile à modifier et à charger en métaux. En raison de son faible coût, il est largement utilisé dans les réactions en phase liquide (par exemple, l'hydrogénation chimique fine) et l'électrocatalyse.
Nanotubes de carbone/Graphène : ces nouveaux matériaux de carbone possèdent une structure de carbone hybride sp² unique, une conductivité extrêmement élevée et des canaux de pores réguliers. Ils induisent non seulement des effets électroniques avec les métaux précieux par conjugaison π-π, mais assurent également un transfert d'électrons rapide pendant l'électrocatalyse grâce à leur conductivité exceptionnelle, démontrant ainsi des performances exceptionnelles dans des domaines tels que les piles à combustible (par exemple, Pt/CNT pour la réduction de l'oxygène) et l'électrolyse de l'eau.
3. Supports en zéolithe
Les zéolithes sont des aluminosilicates cristallins caractérisés principalement par leurs systèmes de canaux microporeux ordonnés et leur acidité réglable.
Sélectivité de forme : La taille des pores à l'échelle moléculaire (généralement <2 nm) permet le passage sélectif des réactifs et des produits en fonction de leur taille et de leur forme, ce qui permet une catalyse sélective en fonction de la forme. Par exemple, dans l'hydrofinissage du diesel catalysé par le Pt/zéolite, les alcènes à chaîne droite peuvent être sélectivement hydrogénés tandis que les alcanes ramifiés sont conservés.
Acidité forte et effet de confinement : Leurs centres fortement acides, combinés au confinement des particules métalliques dans des micropores, leur permettent d'exceller dans des réactions telles que l'isomérisation des alcanes et l'aromatisation.
4. Autres nouveaux supports
Avec les progrès de la nanotechnologie, une gamme de nouveaux supports présente un grand potentiel.
Cadres métallo-organiques (MOF): Composés d'ions métalliques et d'éléments de liaison organiques, ils présentent une surface spécifique très élevée et des environnements poreux pouvant être conçus à l'échelle atomique, ce qui en fait des plateformes idéales pour obtenir une dispersion à un seul atome de métaux précieux et une catalyse sélective en fonction de la taille.
Matériaux mésoporeux : Les matériaux mésoporeux, tels que le SBA-15 et le MCM-41, présentent des structures mésoporeuses très ordonnées et des distributions de tailles de pores étroites, fournissant des canaux idéaux pour le transfert de masse et les réactions de grosses molécules, ce qui permet de résoudre les problèmes de transfert de masse lent posés par les matériaux microporeux.
Carbures/nitrures : Comme le carbure de molybdène et le nitrure de carbone, ils présentent une conductivité semblable à celle des métaux, une grande stabilité chimique et une grande stabilité thermique. En tant que supports d'électrocatalyseurs émergents ou catalyseurs synergiques, ils ont le potentiel de remplacer les supports traditionnels.
Tableau 2 : Comparaison des caractéristiques d'autres types de supports
|
Type de support |
Caractéristique structurelle |
Avantage principal |
Applications potentielles |
|
Zéolithes |
Micro-poreux cristallin |
Sélectivité de forme, forte acidité |
Hydrogénation sélective de la forme, isomérisation, tamisage moléculaire |
|
MOFs |
Cristallins Poreux |
Surface ultra-élevée, structure concevable |
Catalyse à atome unique, stockage/séparation des gaz |
|
Matériaux mésoporeux |
Mésopores ordonnés |
Taille uniforme des pores, efficacité élevée du transfert de masse |
Catalyse de grandes molécules, biodétection |
|
Carbures/Nitrures |
Composés interstitiels |
Conductivité élevée, stabilité élevée |
Électrocatalyse, catalyse résistante à la corrosion |
Chapitre 5 : Défis et perspectives d'avenir
Les catalyseurs à base de métaux précieux, bien qu'indispensables, se heurtent à des obstacles importants qui motivent les recherches en cours. Le principal défi reste leur coût élevé et leur rareté naturelle, ce qui crée des vulnérabilités économiques et de chaîne d'approvisionnement pour les applications à grande échelle telles que la catalyse automobile et la production de produits chimiques en vrac. À cela s'ajoute leur tendance inhérente à se désactiver, principalement par frittage - lorsque les nanoparticules s'agglomèrent en particules plus grandes et moins actives à des températures élevées - et par empoisonnement par des sous-produits de réaction. En outre, les performances de ces catalyseurs sont souvent limitées par les matériaux de support traditionnels qui fonctionnent simplement comme des échafaudages passifs, ne parvenant pas à améliorer ou à stabiliser activement le métal précieux. Un défi scientifique plus profond réside dans la compréhension incomplète des changements dynamiques sur les sites actifs dans des conditions de fonctionnement réelles et des relations structure-activité précises, ce qui entrave la conception rationnelle.
Les progrès futurs sont étroitement liés à des stratégies innovantes qui maximisent l'efficacité et la durabilité. L'accent est mis sur l'optimisation de l'efficacité de l'utilisation de l'atome. Cela implique de dépasser la simple dispersion des nanoparticules pour passer à des architectures avancées telles que les catalyseurs à atome unique (SAC), qui peuvent théoriquement atteindre une dispersion de 100 % des métaux, et des structures sophistiquées de type cœur-coquille ou nanocadre qui concentrent les atomes précieux à la surface où se produisent les réactions. La stratégie d'"extraction d'atomes", par exemple, montre comment la conception d'un alliage peut être utilisée pour attirer les atomes de métaux précieux du cœur d'une nanoparticule vers sa surface, ce qui augmente considérablement l'efficacité tout en minimisant la charge.
Parallèlement, le rôle du support est en train d'être redéfini : de spectateur passif, il devient un partenaire actif et synergique. L'avenir réside dans la conception de supports intelligents capables d'un contrôle électronique et géométrique précis. Il s'agit notamment de concevoir des interactions métal-support fortes (SMSI) pour optimiser les propriétés électroniques et d'utiliser de nouveaux matériaux tels que les cadres métal-organiques (MOF) ou les hydroxydes doubles en couches 2D (LDH) qui offrent des environnements définis au niveau atomique pour stabiliser les atomes métalliques. Le concept des effets de confinement, où les particules métalliques sont physiquement piégées dans des structures poreuses, est une approche puissante pour prévenir le frittage.
Le paradigme de développement passe de la découverte empirique à la conception rationnelle. L'intégration de l'apprentissage automatique, du calcul à haut débit et de la caractérisation in situ avancée accélère la découverte de nouveaux matériaux et notre compréhension des mécanismes catalytiques. Parallèlement à l'optimisation de l'utilisation des métaux précieux, la recherche à long terme de catalyseurs à faible teneur en MGP (métaux du groupe du platine) et, à terme, sans MGP, basés sur des métaux de transition abondants sur terre, reste une voie essentielle, bien que difficile, vers la catalyse durable. Ces efforts combinés visent à rompre les compromis traditionnels entre l'activité, la stabilité et le coût.

Fig. 4 Les nanotechnologies du futur
Chapitre 6 : Conclusion
En résumé, le support joue de multiples rôles dans les catalyseurs à base de métaux précieux qui vont bien au-delà d'un simple échafaudage physique. Il est la pierre angulaire qui permet d'obtenir une forte dispersion, une grande stabilité et une grande efficacité d'utilisation des métaux précieux, et il est essentiel pour améliorer activement les performances catalytiques grâce à des effets électroniques et synergiques. Face aux défis fondamentaux que représentent la rareté et l'instabilité des métaux précieux, l'orientation future est claire : il s'agit de passer du criblage empirique traditionnel à une conception rationnelle précise. En construisant des catalyseurs à un seul atome, des structures cœur-coquille et en développant de nouveaux supports multifonctionnels, nous pouvons "décorer de manière exquise" les métaux précieux à l'échelle atomique/nanométrique. Cela nous permettra en fin de compte de réduire considérablement l'utilisation des métaux précieux tout en améliorant de manière multiplicative les performances catalytiques et la durée de vie, fournissant ainsi la force motrice essentielle pour le développement durable dans les secteurs de l'énergie, de l'environnement et de la chimie.
Pour des solutions avancées de catalyse à base de métaux précieux qui répondent à ces demandes en constante évolution, contactez Stanford Advanced Materials (SAM).
Lire aussi :
La catalyse redéfinie : Avantages du palladium sur carbone
Références :
[1] Bell, A. T. (2003). L'impact de la nanoscience sur la catalyse hétérogène. Science, 299(5613), 1688-1691.
[2] Somorjai, G. A., & Li, Y. (2010). Introduction à la chimie des surfaces et à la catalyse. Wiley.
[3] Tauster, S. J., Fung, S. C., & Garten, R. L. (1978). Strong Metal-Support Interactions. Group 8 Noble Metals Supported on TiO2. Journal of the American Chemical Society, *100*(1), 170-175.
[4] Cargnello, M., et al. (2013). Control of Metal Nanocrystal Size Reveals Metal-Support Interface Role for Ceria Catalysts (Contrôle de la taille des nanocristaux métalliques révèle le rôle de l'interface métal-support pour les catalyseurs à base de cérium). Science, 341(6147), 771-773.

 Barres
Barres
 Perles et sphères
Perles et sphères
 Boulons et écrous
Boulons et écrous
 Creusets
Creusets
 Disques
Disques
 Fibres et tissus
Fibres et tissus
 Films
Films
 Flocon
Flocon
 Mousses
Mousses
 Feuille d'aluminium
Feuille d'aluminium
 Granulés
Granulés
 Nids d'abeilles
Nids d'abeilles
 Encre
Encre
 Stratifié
Stratifié
 Grumeaux
Grumeaux
 Mailles
Mailles
 Film métallisé
Film métallisé
 Assiette
Assiette
 Poudres
Poudres
 Tige
Tige
 Feuilles
Feuilles
 Cristaux simples
Cristaux simples
 Cible de pulvérisation
Cible de pulvérisation
 Tubes
Tubes
 Laveuse
Laveuse
 Fils
Fils
 Convertisseurs et calculatrices
Convertisseurs et calculatrices
 Écrire pour nous
Écrire pour nous
 Dr. Samuel R. Matthews
Dr. Samuel R. Matthews



