Nitrate d'ammonium de cérium(IV) : Un oxydant couramment utilisé
Le nitrate de cérium(IV) et d'ammonium (CAN) est un oxydant couramment utilisé. La formule moléculaire du nitrate de cérium(IV) et d'ammonium est Ce(NH4)2(NO3)6. Il s'agit d'un cristal rouge-orange, soluble dans l'eau et l'éthanol, presque insoluble dans l'acide nitrique concentré et déliquescent dans l'air. Il est souvent utilisé comme oxydant pour la corrosion des circuits et la production d'autres composés contenant du cérium.
%20Ammonium%20Nitrate.jpg)
Nitrate de cérium(IV) et d'ammonium
Le nitrate d'ammonium de cérium(IV) est un oxydant puissant, qui est plus oxydant dans des conditions acides, après F2, XeO3, Ag2+, O3, HN3. Dans des solutions aqueuses et d'autres solvants protiques, le nitrate d'ammonium de cérium(IV) est un oxydant à un électron. La consommation de nitrate de cérium(IV) et d'ammonium peut être évaluée par le changement de couleur (de l'orange au jaune clair).
En raison de la limitation de la solubilité dans les solvants organiques, les réactions impliquées dans le nitrate d'ammonium de cérium(IV) sont principalement effectuées dans des solvants mixtes tels que l'eau/acétonitrile. En présence d'autres oxydants tels que le bromate de sodium, l'hydroperoxyde de tert-butyle et l'oxygène, Ce4+ peut être recyclé pour obtenir une réaction catalytique. En outre, le nitrate d'ammonium de cérium(IV) est également un réactif de nitration efficace.
Le CAN a une activité oxydante sur les composés contenant de l'oxygène tels que les alcools, les phénols et les éthers, parmi lesquels il a des propriétés oxydantes spécifiques sur les alcools secondaires. Par exemple, il oxyde l'alcool benzylique en aldéhydes et cétones correspondants(équation 1). Même l'alcool p-nitrobenzyle peut être oxydé en cétone p-nitrobenzyle par le système d'oxydation catalytique CAN/O2. En outre, pour des alcools secondaires particuliers tels que le 4-énol ou le 5-énol, des composés éthers cycliques(équation 2) peuvent également être obtenus sous l'action du CAN.
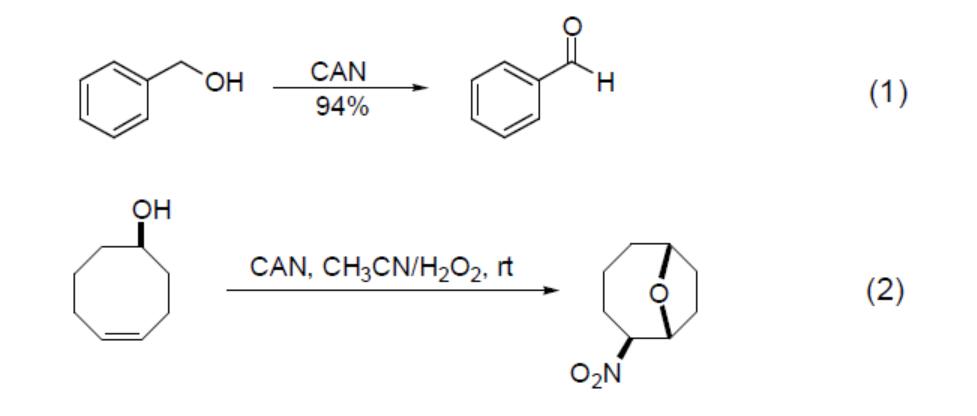
Le catéchol, l'hydroquinone et leurs éthers méthyliques peuvent être oxydés en quinone sous l'action du CAN, comme la conversion du catéchol en o-benzoquinone(équation 3), la conversion rapide de l'hydroquinone en p-benzoquinone(équation 4) sous l'action du CAN et des ultrasons, et la conversion des éthers d'aryle en p-benzoquinone.
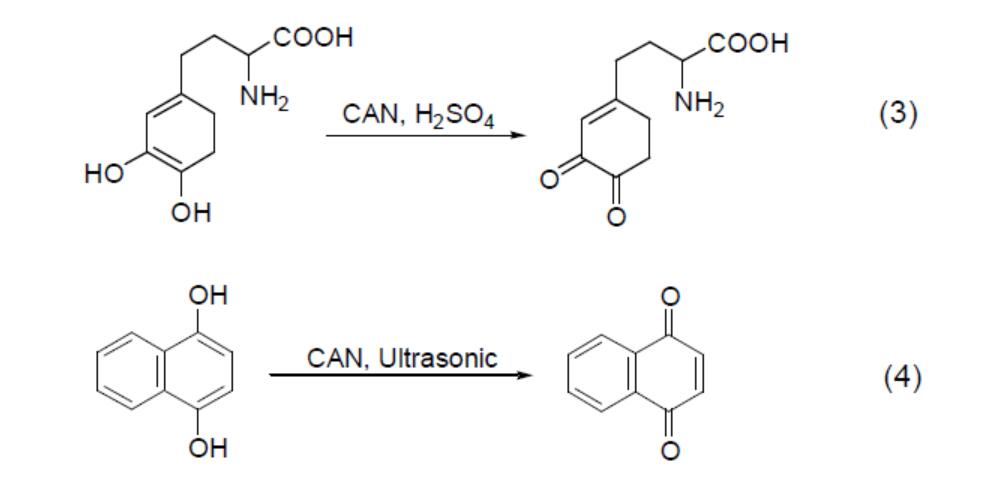
Sa réaction d'oxydation des composés époxydiques peut également produire des composés dicarbonylés(équation 5). En outre, le CAN a également une activité oxydante sur les composés carbonylés ayant des structures spécifiques, comme l'oxydation des cétones à cage polycyclique en lactones(équation 6).
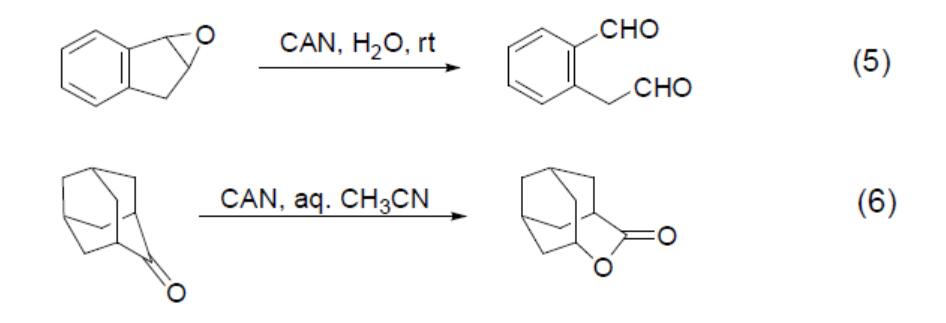
En tant qu'oxydant à un seul électron, le CAN peut également réaliser des réactions de formation de liaisons carbone-carbone intermoléculaires ou intramoléculaires. Par exemple, la réaction d'addition oxydative du composé 1,3-dicarbonyle et du système styrène sous l'action du CAN(équation 7), ou la réaction de dimérisation de l'aniline elle-même(équation 8).
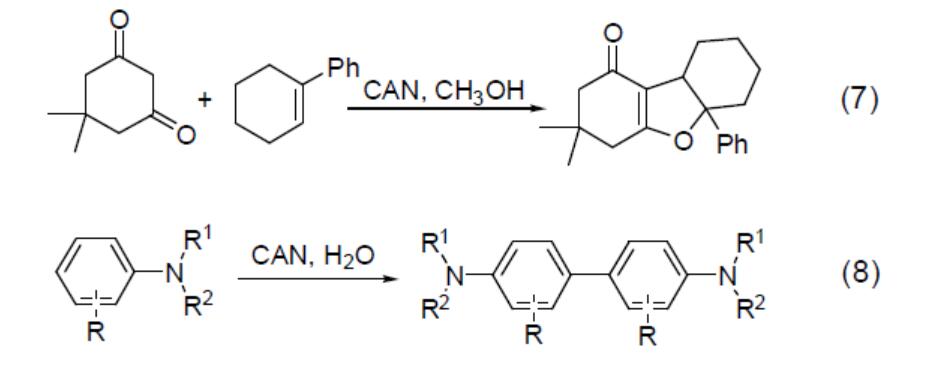
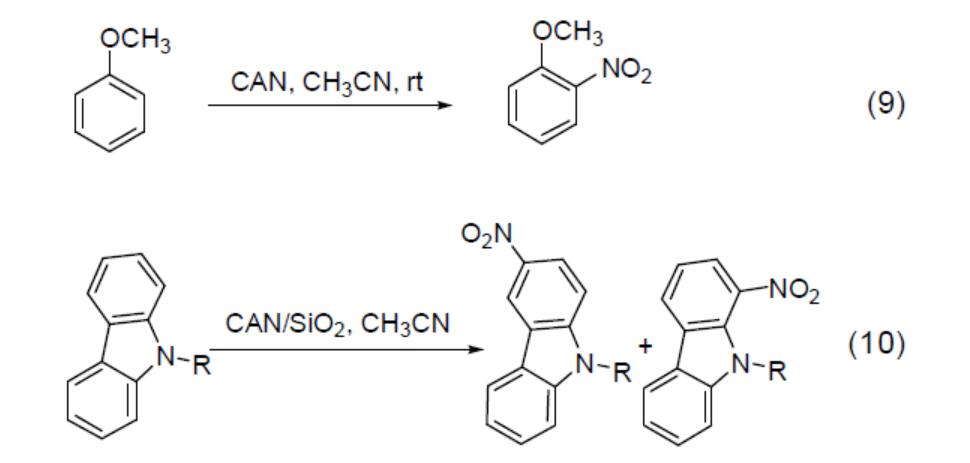
Outre les réactions d'oxydation, le CAN est également un réactif de nitration efficace, en particulier pour la nitration des systèmes de noyaux aromatiques. Par exemple, dans l'acétonitrile, le CAN réagit avec l'anisole pour obtenir des produits d'ortho-nitration(équation 9). Cependant, en raison des fortes propriétés oxydantes du CAN, le système cyclique aromatique subit souvent des réactions de polynitration et produit même des polymères difficiles à séparer.Par exemple, dans l'acétonitrile, l'utilisation du gel de silice comme support pour nitrer le carbazole et le 9-alkylcarbazole avec le CAN permet d'augmenter le rendement de 70 à 80 %(équation 10).
Conclusion
Nous vous remercions d'avoir lu notre article et nous espérons qu'il vous aidera à mieux comprendre le nitrate d'ammonium de cérium(IV), l'oxydant le plus couramment utilisé. Si vous souhaitez en savoir plus sur le nitrate d'ammonium de cérium(IV) et d'autres poudres, nous vous conseillons de visiter le site de Stanford Advanced Materials (SAM) pour plus d'informations.
En tant que fournisseur mondial de produits de nitrate d'ammonium de cérium( IV ), Stanford Advanced Materials (SAM) a plus de deux décennies d'expérience dans la fabrication et la vente de nitrate d'ammonium de cérium(IV), offrant du nitrate d'ammonium de cérium(IV ) de haute qualité pour répondre aux besoins des clients en matière de R&D et de production. Nous sommes convaincus que SAM sera votre fournisseur et partenaire commercial préféré pour le nitrate d'ammonium de cérium( IV) .

 Barres
Barres
 Perles et sphères
Perles et sphères
 Boulons et écrous
Boulons et écrous
 Creusets
Creusets
 Disques
Disques
 Fibres et tissus
Fibres et tissus
 Films
Films
 Flocon
Flocon
 Mousses
Mousses
 Feuille d'aluminium
Feuille d'aluminium
 Granulés
Granulés
 Nids d'abeilles
Nids d'abeilles
 Encre
Encre
 Stratifié
Stratifié
 Grumeaux
Grumeaux
 Mailles
Mailles
 Film métallisé
Film métallisé
 Assiette
Assiette
 Poudres
Poudres
 Tige
Tige
 Feuilles
Feuilles
 Cristaux simples
Cristaux simples
 Cible de pulvérisation
Cible de pulvérisation
 Tubes
Tubes
 Laveuse
Laveuse
 Fils
Fils
 Convertisseurs et calculatrices
Convertisseurs et calculatrices
 Écrire pour nous
Écrire pour nous
 Chin Trento
Chin Trento



