Les alliages à mémoire de forme dans les applications biomédicales
1 Introduction
1.1 Informations générales
Les alliages à mémoire de forme (AMF) sont des matériaux composés de deux éléments métalliques ou plus qui présentent des effets de mémoire de forme (EMF) grâce à la thermoélasticité et aux transformations de phase martensitiques et à leurs inversions. Les alliages à mémoire de forme sont les matériaux qui présentent les meilleures performances de mémoire de forme parmi les matériaux à mémoire de forme. À ce jour, plus de 50 types d'alliages à mémoire de forme ont été découverts.
Les alliages à mémoire de forme présentent des effets de mémoire de forme. Par exemple, lorsqu'un ressort en alliage à mémoire de forme est placé dans de l'eau chaude, sa longueur s'allonge immédiatement. Lorsqu'il est placé dans l'eau froide, il reprend immédiatement sa forme initiale. Les ressorts en alliage à mémoire de forme peuvent être utilisés pour contrôler la température de l'eau dans la plomberie des salles de bains : lorsque la température de l'eau devient trop élevée, la fonction "mémoire" régule ou coupe l'arrivée d'eau pour éviter les brûlures. Ils peuvent également être utilisés pour créer des dispositifs d'alarme incendie et des mécanismes de sécurité pour les équipements électriques. En cas d'incendie, le ressort en alliage à mémoire de forme se déforme, ce qui déclenche le système d'alarme incendie et permet d'atteindre l'objectif d'alerte. En outre, les ressorts en alliage à mémoire de forme peuvent être placés à l'intérieur de vannes de chauffage pour maintenir la température ambiante, en ouvrant ou en fermant automatiquement les vannes lorsque la température devient trop basse ou trop élevée. L'effet de mémoire de forme des alliages à mémoire de forme est également largement appliqué dans divers déclencheurs de capteurs de température.

Fig. 1 Applications médicales du nitinol
Une autre propriété importante des alliages à mémoire de forme est la pseudoélasticité (également connue sous le nom de superélasticité), qui se manifeste par une capacité de récupération de la déformation nettement supérieure à celle des métaux ordinaires sous l'effet d'une force extérieure. En d'autres termes, la déformation importante générée lors de la mise en charge se rétablit lors de la décharge. Cette propriété a trouvé de nombreuses applications en médecine, dans la réduction des vibrations des bâtiments et dans la vie quotidienne. Par exemple, les os artificiels mentionnés ci-dessus, les dispositifs de pression pour la fixation des os et les appareils d'orthodontie dentaire. Les montures de lunettes fabriquées à partir d'alliages à mémoire de forme peuvent supporter des déformations beaucoup plus importantes que les matériaux ordinaires sans se casser (cela n'est pas dû à l'effet de mémoire de forme, où la déformation est suivie d'un chauffage pour restaurer la forme).
Les alliages à mémoire de forme (AMF) ont de nombreuses applications dans le domaine médical clinique, comme les os artificiels, les dispositifs de pression pour la fixation des os, les appareils d'orthodontie dentaire, divers stents endovasculaires, les dispositifs d'embolisation, les dispositifs de réparation cardiaque, les filtres à thrombus, les fils-guides d'intervention et les sutures chirurgicales. Les alliages à mémoire de forme jouent un rôle irremplaçable dans la médecine moderne. Les alliages à mémoire de forme sont également étroitement liés à notre vie quotidienne.
Le développement des alliages à mémoire de forme (AMF) est né de la découverte par Arne Ölander, en 1932, de l'effet "mémoire" des alliages or-cadmium. En 1963, l'équipe de Buehler de l'U.S. Naval Ordnance Laboratory a confirmé ce phénomène dans les alliages de nickel-titane : les matériaux déformés plastiquement en dessous de leur température de transition reprennent spontanément leur forme initiale lorsqu'ils sont chauffés au-dessus d'un seuil critique (par exemple, >40°C), sous l'effet d'une transformation martensitique inverse activée thermiquement. Des percées industrielles ont été réalisées en 1969 avec des raccords de tuyauterie étanches en NiTi pour l'hydraulique aéronautique et une antenne lunaire pré-déformée en NiTi qui s'est auto-expansée sous l'effet du chauffage solaire lors de la mission Apollo 11, surmontant ainsi les contraintes liées à la charge utile. Des recherches ultérieures ont permis de développer des systèmes NiTi multicomposants (par exemple, TiNiCu, TiNiFe) parallèlement aux SMA à base de cuivre et de fer, permettant des applications transformatrices dans les domaines de la biomédecine, de l'énergie et de l'automatisation.
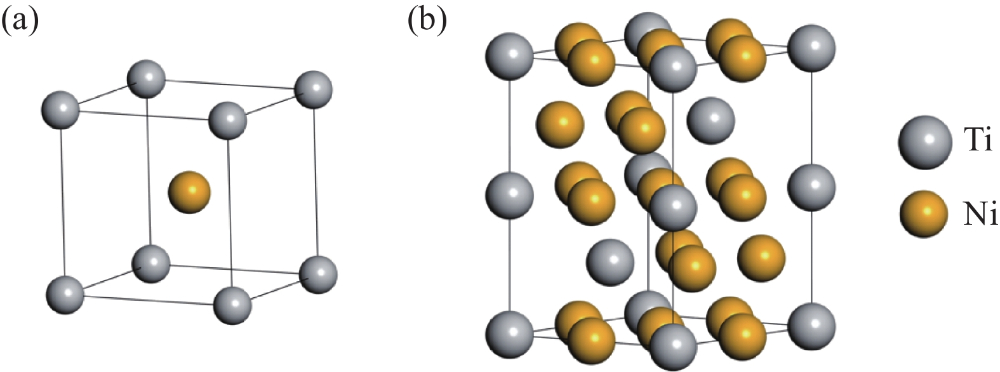
Fig. 2 Structure cristalline du nitinol
L'alliage à mémoire de forme à base de Ti-Ni est le plus utile de tous les types d'alliages à mémoire de forme. Les propriétés uniques des alliages nickel-titane découlent de la transformation de phase réversible entre la phase austénitique (haute température/état non chargé, structure cubique stable) et la phase martensitique (basse température/état chargé, structure hexagonale facilement déformable). Les caractéristiques principales sont les suivantes effet de mémoire de forme (la déformation de la martensite suivie d'un chauffage à la température critique restaure la forme de la phase parentale), superélasticité non linéaire (la transformation de la phase martensite induite par la contrainte permet une déformation récupérable de 8 %, brisant les limites de la loi de Hooke), sensibilité orale à la température (la force orthodontique augmente avec l'augmentation de la température, accélère le mouvement des dents mais rend difficile un contrôle précis), une excellente biocompatibilité (l'oxyde de titane de surface inhibe la libération d'ions de nickel), et une force orthodontique douce qui amortit les vibrations (la plate-forme de la courbe de décharge est plate, l'amplitude des vibrations ne représentant que 50 % de celle d'un fil d'acier inoxydable). Basés sur la régulation de la transformation de phase, les arcs orthodontiques ont évolué sur cinq générations : fils métalliques traditionnels (années 1940) → alliages stabilisés à la martensite (années 1960, faible rigidité, pas de mémoire) → alliages activés austénitiques (années 1980, superélasticité à force constante) → alliages activés martensitiques (années 1990, mémoire de forme et superélasticité déclenchées par la température du corps, réalisant une "activation intraorale à température ambiante") → alliages optimisés thermodynamiquement (années 2000, activés à plus de 40 °C, fournissant une force continue extrêmement faible pour les patients atteints de maladies parodontales).
1.2 L'attrait des SMA dans le domaine médical
L'intérêt des alliages à mémoire de forme (AMF) dans le domaine médical réside dans la synergie unique entre leurs propriétés matérielles et les exigences cliniques.
Les SMA de qualité médicale, représentés par le Nitinol (NiTi), ont une composition quasi équiatomique (50 % de nickel, 50 % de titane). Des ajustements précis de la composition permettent de contrôler les effets de superélasticité et de mémoire de forme. Le nitinol superélastique subit une transformation martensitique induite par la contrainte, ce qui permet d'obtenir des déformations récupérables jusqu'à 8,0 % (Fig. 1). Sa courbe contrainte-déformation présente un plateau distinct, surpassant l'acier inoxydable 316 médical conventionnel.
Les avantages cliniques clés englobent trois dimensions :
1. Innovation fonctionnelle : La superélasticité permet la miniaturisation et l'auto-expansion dans les dispositifs peu invasifs (par exemple, les endoprothèses vasculaires, les filtres) ;
2. Biocompatibilité : Le nitinol à surface optimisée répond aux normes de sécurité biologique pour les implants.
3. Avancement de la chirurgie : Les dispositifs alimentés par SMA (par exemple, les arcs orthodontiques, les occluders cardio-neurovasculaires) améliorent la précision de la procédure tout en réduisant les traumatismes tissulaires.
En radiologie interventionnelle notamment, la superélasticité du Nitinol permet de relever des défis critiques en matière de flexibilité des dispositifs, de résistance au pliage et d'adaptation dynamique in vivo, ce qui entraîne des progrès transformateurs dans les thérapies peu invasives. Cet article examine plus en détail le potentiel d'application médicale de la SMA et les stratégies de gestion des risques pour les implants en nitinol.
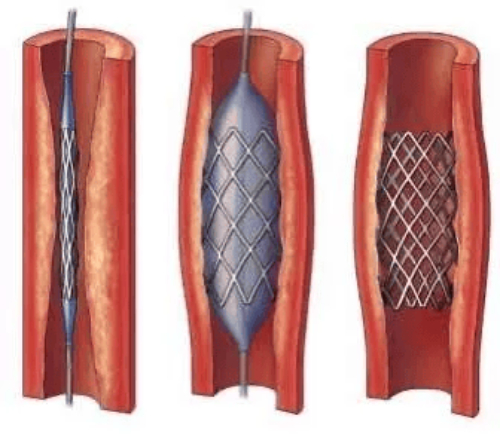
Fig. 3 Déploiement d'une endoprothèse en nitinol
2 Principes fondamentaux des alliages à mémoire de forme utilisés en biomédecine
2.1 Principaux types et composants
Les alliages à base de nickel et de titane, en particulier le nitinol binaire (NiTi) de composition quasi équiatomique (50 % de Ni-Ti), constituent la pierre angulaire des SMA médicaux en raison de leur superélasticité intrinsèque (∼8 % de déformation de récupération) et de leur mémoire de forme activée thermiquement. Les systèmes d'alliages ternaires sont conçus pour répondre aux limitations cliniques : NiTiNb étend l'hystérésis de transformation (ΔT≈30-100°C) pour améliorer la stabilité dimensionnelle des dispositifs de fixation osseuse, en résistant aux fluctuations thermiques ; NiTiCu rétrécit l'hystérésis (ΔT≈2-10°C) pour un contrôle précis de la réponse mécanique, permettant un ajustement de la force radiale à l'échelle du millimètre dans les endoprothèses vasculaires ; NiTiCr élève le potentiel de piqûre (+0,2V) et renforce les couches de passivation pour supprimer la libération d'ions de nickel, atténuant ainsi les risques d'allergie. En revanche, les alliages à base de cuivre (par exemple Cu-Al-Ni, Cu-Zn-Al) offrent une rentabilité et des températures de transition réglables, mais souffrent d'une fragilité intergranulaire (résistance à la fatigue <10^4 cycles) et d'une libération d'ions de cuivre cytotoxiques, ce qui exclut l'utilisation d'implants. Les systèmes à base de fer (par exemple, Fe-Mn-Si) présentent une résistance élevée et un coût abordable ; cependant, leur faible déformation de récupération (<2%) et l'absence de superélasticité réversible limitent leurs applications à des dispositifs exploratoires et non porteurs, sans traduction clinique significative à ce jour.
Tableau 1 Comparaison des propriétés des alliages à mémoire de forme fabriqués à partir de différents matériaux
|
Classification |
Alliages typiques |
Caractéristiques principales Orientation de l'optimisation |
Valeur médicale et limites |
|
Alliage à base de nickel et de titane (à base de NiTi) |
NiTi binaire |
Superélasticité (déformation de récupération de ~8%) Effet de mémoire de forme (déclenchement à température ambiante) |
Matériau clinique courant avec une bonne biocompatibilité (la barrière TiOx de surface empêche la libération de nickel) |
|
Alliage à base de cuivre (à base de cuivre) |
NiTiNb |
Élargissement de la température de décalage de la transition de phase (ΔT≈30-100℃) |
Amélioration de la stabilité dimensionnelle des implants (comme l'anti-desserrage des vis orthopédiques) |
|
NiTiCu |
Réduire l'effet de décalage (ΔT≈2-10℃) |
Amélioration de la précision de la réponse mécanique (force radiale contrôlée des stents vasculaires) |
|
|
NiTiCr |
Résistance accrue à la corrosion (potentiel de piqûre ↑0,2V). Inhibition de la précipitation des ions nickel |
Réduit le risque de toxicité à long terme de l'implant (en particulier pour les patients allergiques au nickel) |
|
|
Cu-Al-Ni |
Faible coût Température de changement de phase élevée (>100℃) |
Limites : Fragilité des limites cristallines → faible durée de vie en fatigue (<10^4 cycles). Toxicité des ions cuivre → inflammation des tissus (interdite cliniquement). |
|
|
Cu-Zn-Al |
Excellente performance de traitement Température de transition de phase réglable (-50~100℃) |
||
|
Alliage à base de fer |
Fe-Mn-Si |
Haute résistance (>500MPa) Faible coût |
Limites : Faible déformation de récupération (<2%) → défaillance fonctionnelle La transition de phase est irréversible → pas de superélasticité (limitée aux dispositifs à usage unique). |
2.2 Caractéristiques et mécanismes fondamentaux
La transformation de phase martensitique est une transformation de phase non diffuse, également connue sous le nom de transformation de phase de type déplacement. Strictement parlant, dans une transformation de phase de type déplacement, on ne peut parler de transformation de phase martensitique que lorsque le déplacement atomique se produit par déformation en cisaillement, que l'interface entre les deux phases est maintenue par déformation élastique macroscopique pour assurer la continuité et la congruence, et que l'énergie de déformation est suffisante pour modifier la cinétique de la transformation de phase et la morphologie des produits de la transformation de phase. Sur la base des définitions de la transformation de phase martensitique proposées par de nombreux chercheurs dans le passé, Xu Zuyao a proposé la définition simple suivante : une transformation de phase dans laquelle les atomes sont remplacés sans diffusion (c'est-à-dire que la composition reste inchangée et que les relations entre les atomes voisins restent inchangées) et sans cisaillement (c'est-à-dire que la phase parentale et la martensite sont dans une relation de position), ce qui modifie leur forme. Ici, la transformation de phase fait référence aux transformations de phase de premier ordre (caractérisées par des changements soudains de chaleur et de volume, tels que les réactions exothermiques et l'expansion) qui impliquent la nucléation et la croissance.
La martensite a été découverte pour la première fois dans l'acier : lorsque l'acier est chauffé à une certaine température puis rapidement refroidi, il forme une structure trempée qui durcit et renforce l'acier. En 1895, le Français Osmont a nommé cette structure martensite en l'honneur du métallurgiste allemand Martens. À l'origine, seule la transformation de phase de l'austénite en martensite dans l'acier était appelée transformation martensitique. Depuis le 20e siècle, des connaissances approfondies ont été accumulées sur les caractéristiques des transformations de phase martensitique dans l'acier. Par la suite, on a découvert que certains métaux et alliages purs présentaient également des transformations de phase martensitique, tels que : Ce, Co, Hf, Hg, La, Li, Ti, Tl, Pu, V, Zr, et Ag-Cd, Ag-Zn, Au-Cd, Au-Mn, Cu-Al, Cu-Sn, Cu-Zn, In-Tl, Ti-Ni, etc. Les produits des transformations de phase dont les caractéristiques de base ressemblent à celles des transformations de phase martensitique sont collectivement appelés martensite.
Les transformations de phase martensitique présentent des effets thermiques et volumétriques, le processus de transformation impliquant la formation et la croissance de noyaux. Cependant, il n'existe pas de modèle complet pour expliquer la formation et la croissance de ces noyaux. Le taux de croissance de la martensite est généralement élevé, certains atteignant jusqu'à 10 cm-s. On suppose que la configuration des défauts cristallins (tels que les dislocations) dans la phase mère influence la nucléation de la martensite. Toutefois, les techniques expérimentales actuelles ne permettent pas d'observer la configuration des dislocations à l'interface des phases, de sorte que l'ensemble du processus de transformation de la phase martensitique reste flou. Ses caractéristiques peuvent être résumées comme suit :
La transformation de phase martensitique est l'une des transformations de phase non diffuse. Au cours de la transformation, il n'y a pas de marche aléatoire ou de saut ordonné des atomes à travers l'interface. Par conséquent, la nouvelle phase (martensite) hérite de la composition chimique, de l'ordre atomique et des défauts cristallins de la phase mère. Au cours de la transformation de la phase martensitique, les atomes subissent un déplacement ordonné tout en conservant leur position relative par rapport aux atomes voisins. Ce déplacement est de type cisaillement. Le résultat du déplacement des atomes est la déformation du réseau. Ce déplacement par cisaillement modifie non seulement la structure du réseau de la phase mère, mais entraîne également des changements de forme macroscopiques. Si une ligne droite est d'abord tracée sur la surface d'un échantillon poli, comme PQRS dans la figure 3a, et qu'une partie de l'échantillon (A1B1C1D1-A2B2C2D2) subit une transformation de phase martensitique (formation de martensite), la ligne droite PQRS est alors pliée en trois lignes droites connectées : PQ, QR' et R'S'. Les plans A1B1C1D1 et A2B2C2D2 à l'interface biphasée restent sans déformation ni rotation, et sont appelés plan habituel (de précipitation). Ce changement de forme est appelé déformation plane constante (figure 3). Le changement de forme entraîne la formation de protubérances à la surface de l'échantillon, qui a été préalablement poli. Les protubérances superficielles de la martensite dans l'acier à haute teneur en carbone peuvent être observées lors de la formation de la martensite, le basculement se produisant sur la surface croisant la martensite. Un microscope interférentiel permet de voir la hauteur des protubérances et leurs arêtes vives.
L'effet de mémoire de forme fait référence au phénomène selon lequel, après déformation d'un alliage qui subit une transformation de phase martensitique, lorsqu'il est chauffé à la température d'achèvement de la transformation de la phase austénitique (Af), la martensite à basse température s'inverse en phase parentale à haute température et reprend sa forme initiale avant déformation, ou lors d'un refroidissement ultérieur, elle reprend la forme de la martensite grâce à la libération de l'énergie élastique interne. Il s'agit d'un matériau solide ayant une certaine forme qui, après avoir subi une déformation plastique dans certaines conditions, reprend complètement sa forme initiale avant déformation lorsqu'il est chauffé à une certaine température. En d'autres termes, il peut conserver la forme de la phase parentale.
La transformation martensitique constitue le fondement physique de l'effet de mémoire de forme par le biais d'un mécanisme thermoélastique de reconstruction cristalline réversible. Lors du refroidissement en dessous de la température de démarrage de la martensite (Ms), la phase austénitique à haute température (réseau cubique) subit un cisaillement sans diffusion pour former de la martensite métastable (réseau monoclinique/hexagonal), générant des jumeaux auto-accommodants sans changement de forme macroscopique. Une contrainte externe inférieure à Mf induit une migration de la frontière entre les jumeaux et une réorientation des variantes, ce qui entraîne des déformations pseudo-plastiques allant jusqu'à 8 %. Un chauffage ultérieur au-dessus de la température de départ de l'austénite (As) déclenche un déplacement coopératif atomique pour une transformation inverse, où la récupération de la structure cristalline entraîne une restauration de la forme macroscopique - l'essence même de l'effet de mémoire de forme. Ce processus repose sur trois attributs essentiels :
① la réversibilité (l'énergie de distorsion du réseau ΔG proche de zéro garantit l'unicité du chemin) ;
② Hystérésis étroite (10-30°C dans les alliages NiTi permettent une activation précise à la température du corps) ;
③ Déformation non destructive (le jumelage remplace le glissement des dislocations pour éviter les dommages permanents). Sur le plan médical, ce mécanisme permet aux endoprothèses auto-expansibles de retrouver des configurations prédéfinies à la température du corps, tandis que le réarrangement martensitique des jumeaux absorbe les vibrations des charges physiologiques (par exemple, amortissement 50 % plus élevé dans les fils orthodontiques). Sa stabilité cyclique (>10^7 cycles) garantit en outre la fiabilité à long terme d'implants tels que les valves cardiaques.
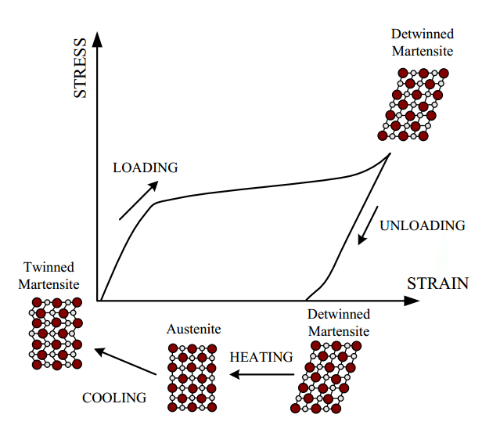
Fig. 4 Effet de mémoire de forme
2.3 Paramètres de performance clés
La viabilité clinique des alliages NiTi médicaux dépend de la synergie entre la biocompatibilité, les propriétés mécaniques, les procédés de fabrication et la compatibilité avec la stérilisation. Selon la norme ISO 10993, la biocompatibilité se concentre sur la suppression de la libération d'ions nickel (la passivation de surface au TiO2 réduit la lixiviation à <0,1 μg/cm^2/semaine), validée par la cytotoxicité (>90% de viabilité cellulaire), la sensibilisation (≥95% de tests épicutanés négatifs) et l'hémolyse (<5%). Les propriétés mécaniques doivent s'aligner sur les exigences de l'implantation : les endoprothèses cardiovasculaires nécessitent une résistance à la fatigue par flexion rotative très élevée (>4×10^8 cycles à 37°C), tandis que les implants articulaires exigent une résistance à l'usure (<0,1 mm3/Mc taux d'usure) ; la rigidité superélastique (0,5-3 GPa) doit correspondre précisément à la mécanique du tissu hôte. La fabrication fait appel à la refonte sous vide (VAR) pour améliorer la pureté (taille des inclusions ≤5 μm), à l'étirage à froid + au vieillissement pour ajuster les températures de transformation (Af±2°C), et à la découpe au laser/électropolissage pour obtenir des caractéristiques à l'échelle du micron (tiges de stent 80-150 μm) avec une faible rugosité (Ra<0,05 μm). La stérilisation terminale (oxyde d'éthylène/irradiation gamma) doit limiter la dérive de la transition de phase à <1°C sans compromis fonctionnel.
3 Applications dans le domaine biomédical
3.1 Orthopédie
Actuellement, la chirurgie orthopédique utilise principalement des plaques d'acier fixes en alliage de titane. Cependant, l'alliage de titane n'a pas de propriétés auto-adaptatives et superélastiques, et son adaptation aux os n'est pas optimale. En revanche, les alliages à mémoire de forme nickel-titane imprimés en 4D, grâce à leurs capacités d'auto-adaptation, peuvent s'adapter relativement parfaitement aux os tout en assurant à la fois des fonctions de soutien et de réparation.
Ces matériaux de réparation orthopédique en alliage à mémoire de forme ne sont pas de simples plaques plates ; leurs surfaces sont densément perforées de minuscules trous, ce qui facilite l'échange de nutriments et favorise la croissance et la réparation des os. De multiples composants adaptatifs en nickel-titane imprimés en 4D ont été implantés cliniquement chez des patients volontaires atteints de tumeurs osseuses, avec des résultats cliniques prometteurs.
Pour la réparation des défauts osseux, des échafaudages en NiTi à structure poreuse graduelle sont utilisés, avec une résistance à la traction de 625,6 MPa, un taux d'élongation de 14,67 % et un taux de récupération de la déformation de 99,51 %. Le renforcement des grains fins (taille des grains ~20,5 μm) est en synergie avec la densité de dislocation pour obtenir une absorption d'énergie sous forte contrainte. Remplacement et réparation des articulations : dispositifs de fixation du cotyle, composants d'articulations artificielles (en cours d'exploration, axée sur l'usure et la fatigue) et comblement des défauts osseux (SMA poreux).
Dans le domaine de la chirurgie de la colonne vertébrale, les alliages à mémoire de forme (AMF), en particulier les alliages nickel-titane (NiTi), ont été à l'origine d'innovations dans le domaine de l'orthopédie dynamique et des techniques de fusion peu invasives. Les tiges orthopédiques en NiTi permettent une correction précise grâce à un effet de mémoire de forme en deux étapes : à basse température, dans la phase martensitique, les tiges subissent une déformation plastique pour s'adapter aux procédures chirurgicales ; une fois implantées dans le corps, la température du corps déclenche une transformation de la phase austénitique, rétablissant la courbure prédéfinie et appliquant continuellement une force de correction axiale (par exemple, une tige de 6 mm de diamètre génère une force d'environ 200 N à 40 °C, tandis qu'une tige de 9 mm atteint 500 N). Des expériences sur des animaux (modèles de chèvres) ont montré que les tiges de NiTi précourbées pouvaient réduire les angles de scoliose de 41° à 11° sans causer de lésions nerveuses ; des études sur des cadavres humains ont confirmé leur capacité à corriger simultanément les déformations coronales, sagittales et rotatoires. En termes de conception de l'innovation clinique, les tiges rectangulaires/carrées améliorent la capacité anti-rotationnelle, corrigeant l'angle de Cobb de 57,8° à 17,8° sans récidive observée sur une période de suivi de 4 ans ; le système déclenché par la température du corps utilise des impulsions de radiofréquence (450 Hz) pour induire un chauffage local, évitant ainsi les risques associés aux dommages thermiques traditionnels.
Le développement de dispositifs de fusion intervertébrale est axé sur une implantation peu invasive et une stabilité à long terme. Grâce aux propriétés de transformation de phase du NiTi, le dispositif de fusion peut subir une déformation par compression dans un état martensitique à basse température (par exemple, dans un environnement d'eau glacée) et retrouver automatiquement sa hauteur initiale après l'implantation dans l'espace intervertébral grâce à une transformation de phase austénitique déclenchée par la température du corps. En ce qui concerne l'optimisation de la structure poreuse, les réseaux en forme de diamant (porosité de 70 à 72 %, réseau unitaire de 1,5 mm) produits à l'aide de la technologie de fusion sélective par laser (SLM) favorisent considérablement la croissance vasculaire. La zone de contact est conçue avec une phase martensitique (faible module d'élasticité) pour réduire efficacement le stress shielding de la plaque terminale. En outre, la structure des "dents de verrouillage" sur les bords du dispositif de fusion s'insère dans les plaques terminales pendant la reprise de forme, atteignant une résistance anti-déplacement de 1800 N, éliminant le besoin de vis ou de tiges auxiliaires pour la fixation et simplifiant davantage la procédure chirurgicale.
Dans le domaine du traitement des fractures, les alliages à mémoire de forme (AMF) ont considérablement amélioré les résultats de la fixation et le pronostic des patients grâce à la compression dynamique, à l'implantation peu invasive et à la technologie d'adaptation biomécanique. Les clous intramédullaires à compression continue utilisent l'effet de mémoire de forme à deux niveaux de l'alliage NiTi. Après avoir été pré-déformés à l'état martensitique à basse température, ils sont implantés dans la cavité médullaire. Lorsqu'ils sont réchauffés à la température du corps, ils reprennent leur forme originale et génèrent une contrainte de compression axiale (0,5-1 MPa), accélérant ainsi la formation du cal osseux. Des études cliniques comparatives montrent que, par rapport aux plaques d'acier traditionnelles, le groupe de clous intramédullaires en NiTi réduit le temps de guérison des fractures de 25 % et le taux de non-union à 0,9 %. Ses caractéristiques peu invasives (par exemple, implantation par une incision de 2 cm pour les fractures des membres pédiatriques, avec un diamètre choisi aux 2/5 du point le plus étroit de la cavité médullaire) améliorent encore de 30 % l'amplitude de mouvement postopératoire de l'articulation.
Les vis à os autocomprimées et les greffes osseuses assurent une fixation active grâce à un mécanisme de changement de phase. La vis osseuse est vissée dans l'os à l'état martensitique et, après réchauffement, elle se dilate radialement, augmentant la contrainte d'interface de 40 % et améliorant de manière significative la force de maintien ; lorsque le fixateur à anneau en TiNi est utilisé pour la fixation sternale, le score de douleur VAS postopératoire diminue à 5,17 ± 1,14 (7,65 ± 1,08 dans le groupe traditionnel). Le séjour à l'hôpital est raccourci de 6 jours. En outre, les fixateurs osseux en alliage de magnésium biodégradable (avec un module d'élasticité de 45 GPa, similaire à celui de l'os cortical) s'alignent sur le cycle de guérison osseuse (taux de guérison de 100 % après 6 mois de suivi), ce qui élimine la nécessité d'une chirurgie d'ablation secondaire et ouvre une nouvelle voie pour l'application pratique des matériaux biodégradables dans la fixation des fractures.
Les plaques de compression à verrouillage (LCP) optimisées par le NiTi ont permis de résoudre les problèmes de fixation chez les patients ostéoporotiques grâce à une conception biomécanique adaptée. Les plaques revêtues de NiTi permettent un verrouillage cortical unique (deux vis de chaque côté des extrémités de la fracture), réduisant la densité des vis de 50 %, et comblent les zones comminutives grâce à l'effet "échafaudage de fixation interne" ; combinées à la technologie d'implantation mini-invasive (MIPPO), les plaques LCP pré-pliées sont insérées sous-musculairement et verrouillées avec des vis percutanées, réduisant la perturbation de l'apport sanguin de 70 %, ce qui convient particulièrement aux fractures dans les zones à faible apport sanguin telles que le tibia distal.
Les alliages à mémoire de forme (AMF) ont réalisé des progrès décisifs en orthopédie, de la correction dynamique à la biocompatibilité, grâce à leur effet de mémoire de forme unique et à leur superélasticité. Dans la correction de la colonne vertébrale, les alliages NiTi permettent un traitement précis grâce à un effet de mémoire de forme en deux étapes : des tiges de correction présentant une déformation plastique à l'état martensitique à basse température sont implantées dans des tunnels sous-cutanés, et la température du corps déclenche une transformation de la phase austénitique pour restaurer la courbure prédéfinie, générant une force de correction axiale de 200 à 500 N (diamètre de 6 à 9 mm). Associé à une conception rectangulaire/carrée pour améliorer la capacité anti-rotationnelle (par exemple, le système Wang réduit l'angle de Cobb de 57,8° à 17,8°), il corrige simultanément les déformations coronales, sagittales et rotationnelles ; la technologie de chauffage par impulsion radiofréquence (450 Hz) minimise encore le risque de lésion thermique. Les dispositifs de fusion intervertébrale utilisent les propriétés de transformation de phase pour une implantation peu invasive : après une compression à basse température, le volume diminue de 40 %, et après l'implantation dans l'espace intervertébral, la hauteur se rétablit automatiquement ; la structure poreuse en forme de diamant (porosité de 70-72 %) préparée par fusion sélective au laser favorise la croissance vasculaire, la zone de contact martensitique réduit la protection contre les contraintes de la plaque terminale, et les "dents de verrouillage" du bord offrent une résistance antidéplacement de 1800 N sans qu'il soit nécessaire de recourir à des fixations auxiliaires.
Dans le domaine de la fixation des fractures, les SMA optimisent considérablement l'efficacité thérapeutique grâce à la compression dynamique et à l'adaptation biomécanique. Les clous intramédullaires pré-déformés en NiTi reviennent à leur état d'origine à la température du corps, générant une contrainte de compression axiale de 0,5-1 MPa, accélérant la formation du cal (temps de guérison réduit de 25 %, taux de non-union de 0,9 %) ; les clous intramédullaires élastiques implantés par une incision de 2 cm dans des fractures de membres pédiatriques améliorent l'amplitude de mouvement de l'articulation de 30 % en postopératoire. Les vis osseuses d'autocompression utilisent la transformation de la phase martensite-austenite pour réaliser l'expansion radiale (la contrainte d'interface a augmenté de 40 %) ; les fixateurs annulaires en TiNi réduisent les scores VAS à 5,17 ± 1,14 après la chirurgie de fixation sternale (groupe traditionnel : 7,65 ± 1,08), avec une réduction de 6 jours du séjour à l'hôpital ; les fixateurs osseux en alliage de magnésium biodégradable (module d'élasticité de 45 GPa) sont complètement absorbés en 6 mois, atteignant un taux de guérison de 100 % et évitant la nécessité d'une intervention chirurgicale secondaire. Les plaques de compression à verrouillage optimisé NiTi réduisent la densité des vis de 50 % grâce à un verrouillage cortical unique (pour les patients ostéoporotiques) et, combinées à la technologie MIPPO, réduisent l'interruption de l'apport sanguin de 70 %, ce qui les rend adaptées aux fractures complexes telles que les fractures du tibia distal.
Les principaux avantages résident dans l'intégration profonde des propriétés des matériaux et des besoins cliniques : l'implantation peu invasive (tiges de correction vertébrale via des tunnels sous-cutanés, dispositifs de fusion avec un volume réduit de 40 %) réduit le risque de lésion nerveuse ; la contrainte de compression dynamique (expression de BMP-2 multipliée par 2) et l'amortissement superélastique (amplitude de vibration de 50 % par rapport à l'acier inoxydable) optimisent le microenvironnement de guérison osseuse ; les dispositifs de fusion en NiTi poreux (module élastique de 25 à 90 GPa) et les alliages de magnésium biodégradables (transfert de charge de 100 % au nouvel os) réduisent de manière significative le stress shielding. Ces innovations permettent de passer d'une fixation passive à une régulation active et d'un support rigide à la biocompatibilité grâce à des mécanismes de changement de phase, à l'optimisation structurelle et à la technologie biodégradable, offrant ainsi des solutions plus sûres et plus efficaces pour le traitement des maladies complexes du squelette.
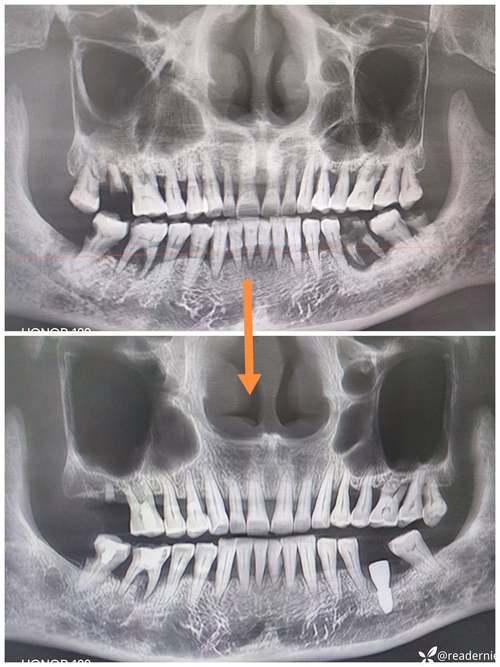
Fig. 5 Radiographie d'une scoliose avec tige rachidienne en nitinol
3.2 Interventions cardiovasculaires
Dans le domaine des interventions cardiovasculaires, les alliages à mémoire de forme (AMF) ont été à l'origine d'innovations technologiques dans le domaine des endoprothèses vasculaires, des occludeurs et des filtres en tirant parti de leur superélasticité et de leurs effets de mémoire de forme. Les endoprothèses vasculaires auto-expansibles, une application typique de la superélasticité, exploitent les propriétés de transformation de phase des alliages NiTi pour permettre un traitement peu invasif : l'endoprothèse est comprimée dans le système de distribution (diamètre de 1 à 2 mm) dans son état martensitique à basse température, puis acheminée par un cathéter jusqu'au site affecté. La température du corps déclenche la transformation de la phase austénitique, ce qui permet au stent de retrouver automatiquement son diamètre prédéfini (par exemple, force d'appui radiale de 0,35 N/mm pour les stents coronaires), éliminant ainsi la nécessité d'une expansion par ballonnet à haute pression. Sa flexibilité est optimisée par des procédés de découpe au laser ou de tissage, avec une rigidité à la flexion aussi faible que 0,3-0,5 N-m^2, ce qui permet de l'adapter à des structures anatomiques complexes telles que la crosse aortique. En outre, la résistance à la fatigue des alliages NiTi (par exemple, l'endoprothèse Eduratec résiste à 100 millions de cycles pulsatiles) garantit une stabilité à long terme, ce qui permet de l'utiliser à différents endroits, notamment dans les vaisseaux périphériques, les artères coronaires, les vaisseaux cérébraux et l'aorte.
L'occluseur utilise l'effet de mémoire de forme à deux phases de la SMA pour réaliser un traitement précis : Les occludeurs de la communication interauriculaire, du foramen ovale ou du canal artériel sont de forme linéaire à l'état martensitique à basse température. Après avoir été introduits dans la cavité cardiaque par un cathéter, la température du corps déclenche leur restauration en une structure disque-taille-disque, la taille étant intégrée dans le site de la malformation et les deux disques ancrant les côtés gauche et droit de l'oreillette/de l'artère, ce qui permet une occlusion peu invasive. Les données cliniques montrent que les occludeurs NiTi peuvent réduire les scores de douleur postopératoire VAS chez les patients présentant une persistance du canal artériel à 2,1 ± 0,8 (par rapport à 5,3 ± 1,2 avec la chirurgie traditionnelle) et raccourcir les séjours à l'hôpital à 3 jours. Leur conception superélastique (avec un taux de récupération de la déformation de 99,2 %) peut s'adapter à la déformation dynamique de la contraction et de la relaxation cardiaques, réduisant ainsi le risque de shunt résiduel.
Le filtre de la veine cave inférieure optimise le traitement de la thromboembolie veineuse grâce à la résistance à la flexion de l'alliage NiTi et à sa capacité de capture du thrombus : le filtre reste comprimé à l'intérieur de la gaine et, lorsqu'il est relâché, il s'appuie sur sa superélasticité pour restaurer sa structure en forme de parapluie. L'ouverture des mailles du filtre (typiquement 1 à 2 mm) peut intercepter plus de 95 % des thrombus tout en permettant une circulation sanguine normale. La durée de vie de l'alliage NiTi (par exemple, taux de fracture du filtre <1% après 5 ans de suivi) garantit la sécurité à long terme, tandis que son faible module d'élasticité (40-60 GPa) réduit l'irritation de la paroi vasculaire et l'incidence de la phlébite.
Ces dispositifs permettent de passer d'un soutien passif à une adaptation active et d'une chirurgie ouverte à une intervention peu invasive grâce au mécanisme de changement de phase et à l'optimisation structurelle du SMA. Leurs principaux avantages sont les suivants : un équilibre entre la flexibilité et la force de soutien radiale grâce à la superélasticité (par exemple, rigidité de flexion du stent coronaire de 0,4 N-m^2, force radiale de 0,35 N/mm), un positionnement et un déploiement précis grâce aux effets de la mémoire de forme (par exemple, erreur de positionnement de l'occluder <1 mm) et une stabilité à long terme grâce à l'adaptation biomécanique (par exemple, taux de perméabilité du filtre de 98 % après 5 ans). Ces innovations offrent des options de traitement plus sûres et plus efficaces pour les maladies cardiovasculaires.
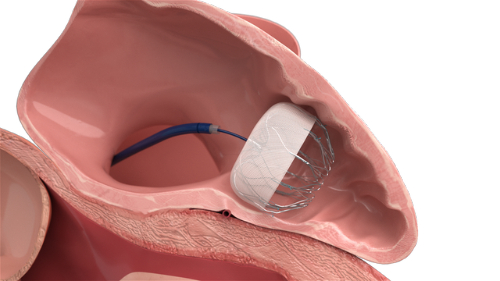
Fig. 6 Occluseur cardiaque
3.3 Médecine dentaire
Dans le domaine de la médecine bucco-dentaire, les alliages à mémoire de forme (AMF) ont été à l'origine d'innovations technologiques en orthodontie, en endodontie, en prosthodontie et en chirurgie maxillo-faciale en raison de leur superélasticité et de leur biocompatibilité. Les arcs orthodontiques, l'une des applications les plus établies, utilisent la superélasticité des alliages NiTi pour fournir des forces correctives continues et douces (0,5-1,5 N), réduisant de manière significative la fréquence des visites de suivi (les données cliniques montrent que les intervalles de suivi peuvent être étendus à 8-12 semaines, soit une amélioration de 40% par rapport aux fils traditionnels en acier inoxydable) tout en améliorant le confort du patient (les scores de l'échelle visuelle analogique [EVA] ont été réduits à 2,3 ± 0,6, contre 4,8 ± 1,1 pour les fils traditionnels). Les fils ayant différentes températures de transition de phase peuvent être adaptés aux différentes étapes du traitement : les fils en phase martensitique à basse température (Af < 25°C) conviennent à l'étape initiale d'alignement, utilisant une faible rigidité (module d'élasticité de 28 GPa) pour réduire les lésions du ligament parodontal ; les fils en phase austénitique (Af > 35°C) fournissent une force orthodontique stable aux étapes ultérieures, garantissant l'efficacité du traitement grâce à un taux de récupération de la déformation de 99,3 %.
Les limes canalaires en NiTi optimisent la sécurité du traitement grâce à leur superélasticité : Les limes traditionnelles en acier inoxydable, en raison de leur grande rigidité, sont sujettes à la déviation du canal radiculaire (taux d'incidence de 12 à 18 %) et à la rupture de l'aiguille (risque de 3 à 5 %). En revanche, les propriétés de transformation de phase martensitique des limes NiTi multiplient par trois la flexibilité dans les canaux radiculaires courbés, ce qui permet de s'adapter à des canaux dont la courbure dépasse 30° et de réduire considérablement les taux de déviation (<2 %) et de rupture d'aiguille (<0,5 %). Des études cliniques montrent que le taux de réussite du traitement du canal radiculaire en une seule visite à l'aide de limes en NiTi atteint 92 %, soit une amélioration de 25 % par rapport aux limes en acier inoxydable, ce qui convient particulièrement aux canaux radiculaires calcifiés ou étroits.
Les crochets et les connecteurs en NiTi utilisés pour la restauration des prothèses dentaires permettent d'obtenir un équilibre entre la force de rétention et le confort grâce à leur superélasticité : Le fermoir est facile à ajuster à l'état martensitique à basse température et reprend sa forme prédéfinie après réchauffement grâce à la transformation de la phase austénitique, ce qui augmente la force de rétention à 3-5 N (contre 1-2 N pour les alliages traditionnels cobalt-chrome). En outre, le faible module d'élasticité (40-60 GPa) réduit la pression sur les gencives (distribution plus uniforme de la pression, avec une réduction de 60 % de l'indice d'irritation des muqueuses). Le connecteur présente une structure tissée avec une excellente résistance à la fatigue (aucune fracture après 10^5 cycles), ce qui le rend approprié pour les systèmes de fixation de précision dans les prothèses partielles amovibles.
En chirurgie maxillo-faciale, les attelles de fixation des fractures et les dispositifs de traction utilisent l'effet de mémoire de forme de la SMA pour un traitement peu invasif : l'attelle est façonnée à basse température pour se conformer à la surface de l'os et, lors du réchauffement, la transformation de phase génère une force de fixation de 50 à 100 N, évitant les dommages aux tissus mous causés par la ligature traditionnelle des fils ; le dispositif de traction réalise un ajustement progressif du segment osseux grâce à un contrôle périodique de la température (par exemple, activation à 40°C et relaxation à 20°C). Les cas cliniques montrent que le temps de guérison des fractures mandibulaires est réduit à 6 semaines (8-10 semaines avec les méthodes traditionnelles), et qu'aucune chirurgie secondaire n'est nécessaire pour retirer les dispositifs de fixation interne.
Les applications susmentionnées permettent de passer d'une adaptation passive à une régulation active et de dispositifs rigides à une adaptation flexible grâce à l'intégration profonde du mécanisme de transition de phase de la SMA aux besoins cliniques. Ses principaux avantages sont les suivants : force douce et soutenue fournie par la superélasticité (erreur de force de correction orthodontique <0,2 N), récupération précise de la forme grâce aux effets de la mémoire de forme (erreur de positionnement de l'anneau <0,5 mm) et sécurité accrue du traitement grâce à l'adaptation biomécanique (taux de rupture de l'aiguille pour le traitement du canal radiculaire <0,5 %). Ces innovations offrent des solutions plus efficaces et plus confortables pour le traitement des maladies bucco-dentaires.

Fig. 7 Lime endodontique en nitinol
3.4 Radiologie interventionnelle et chirurgie mini-invasive
Dans les procédures interventionnelles et les opérations chirurgicales peu invasives, les alliages à mémoire de forme (AMF) améliorent considérablement la maniabilité et l'adaptabilité des dispositifs médicaux grâce à leur superélasticité et à leurs effets de mémoire de forme. Les fils-guides et les cathéters superélastiques, qui tirent parti des propriétés de transformation de phase des alliages NiTi, présentent des performances exceptionnelles dans les structures anatomiques complexes : Les fils-guides présentent une grande flexibilité (rayon de courbure <1 mm) à l'état martensitique à basse température, ce qui permet de s'adapter à la spirale de 360° des artères coronaires ; après le réchauffement, la transformation de la phase austénitique confère une grande résistance à la rupture (déformation à la rupture >8%), associée à la forme en "J" à l'extrémité distale du fil-guide, ce qui permet un contrôle précis du couple (efficacité de la transmission du couple jusqu'à 95%). Le cathéter optimise la flexibilité de l'extrémité grâce à la technologie de découpe au laser, ce qui permet à un cathéter 5F de traverser en douceur le segment tortueux de l'artère carotide (rayon de courbure de 2 mm). L'échafaudage super-élastique fournit un support suffisant (résistance axiale de 12 N) pour éviter les lésions vasculaires causées par l'effet "bouche de poisson".
Les instruments de préhension et d'extraction des calculs, tels que les paniers à calculs et les pinces à corps étrangers, utilisent l'effet de mémoire de forme à deux niveaux de la SMA pour les procédures peu invasives : Les instruments conservent une forme linéaire droite à l'état martensitique à basse température. Après avoir été acheminés vers le site cible via le canal endoscopique, la température du corps déclenche leur restauration à la structure de panier préétablie (par exemple, conception à quatre griffes), ce qui permet de récupérer des pierres ou des corps étrangers d'un diamètre allant de 2 à 10 mm. Le taux de récupération de la souche atteint 99,5 %, ce qui garantit un taux de réussite de l'extraction unique supérieur à 90 %. Les données cliniques montrent que la lithotritie urétéroscopique (URSL) utilisant des paniers à calculs en NiTi réduit la durée de l'intervention à 25 minutes (contre 40 minutes avec les méthodes traditionnelles), avec un taux de calculs résiduels post-opératoires <5%.
Les bobines d'embolisation d'anévrisme optimisent l'efficacité de l'emballage grâce à des effets de mémoire de forme partielle : Les spires sont comprimées dans le microcathéter (diamètre de 0,015-0,021 pouces) et s'adaptent à la morphologie de la cavité de l'anévrisme grâce à leur superélasticité (densité d'empaquetage >30%). En outre, la force de rappel générée par la transformation de la phase martensitique réduit le risque de déplacement de la bobine (taux de récurrence <2% à un an de suivi). Pour les anévrismes à large col, les bobines de NiTi avec une structure tissée tridimensionnelle peuvent former un "panier" stable, associé à la technologie de l'assistance par stent, pour augmenter la densité d'embolisation jusqu'à 95 %.
Les endoscopes déformables et les écarteurs auto-expansifs simplifient le processus chirurgical grâce à la capacité de déformation active de SMA : la section d'insertion de l'endoscope utilise une structure de tube en spirale en alliage de NiTi qui revient automatiquement à un angle de flexion prédéfini (par exemple, 90°) à la température du corps, réduisant ainsi les risques de blessures, 90°) à la température du corps, ce qui réduit la nécessité pour le chirurgien d'ajuster manuellement la courbure ; l'écarteur auto-expansif est comprimé et chargé à basse température et, lorsqu'il est relâché, il élargit rapidement le champ opératoire en utilisant la superélasticité (temps d'expansion <5 secondes), évitant la compression continue des tissus causée par les écarteurs traditionnels (avec une amélioration de 40 % de l'uniformité de la distribution de la pression). Ces conceptions augmentent l'espace opérationnel de 30 % pour la cholécystectomie laparoscopique (LC) et d'autres interventions chirurgicales, réduisant la durée de l'opération à 35 minutes (50 minutes avec les méthodes traditionnelles).
Les instruments susmentionnés permettent de passer d'un fonctionnement passif à une adaptation active et d'un contrôle linéaire à une régulation tridimensionnelle grâce à l'intégration profonde du mécanisme de changement de phase de SMA aux besoins cliniques. Leurs principaux avantages sont les suivants : une combinaison équilibrée de propriétés anti-pliage et de flexibilité grâce à la superélasticité (tension de rupture du fil de 8 % contre 3 % pour l'acier inoxydable), une récupération précise de la forme grâce aux effets de la mémoire de forme (erreur de positionnement du panier de pierres < 1 mm) et des effets peu invasifs grâce à l'adaptation biomécanique (diamètre d'insertion de l'endoscope réduit à 2,8 mm). Ces innovations offrent des solutions plus sûres et plus efficaces pour les procédures interventionnelles et chirurgicales complexes.
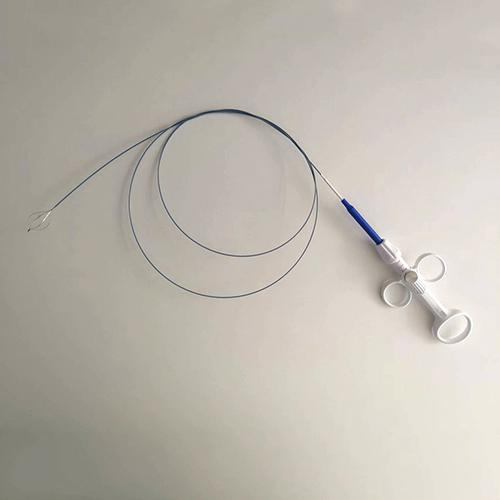
Fig. 8 Panier de pierres en nitinol
6 Conclusion
Les alliages à mémoire de forme (AMF), en particulier les alliages nickel-titane (NiTi), présentent une valeur unique et irremplaçable dans le domaine médical en raison de leur superélasticité et de leur effet de mémoire de forme (EMF). Leur superélasticité permet d'exercer des forces correctrices soutenues et douces - par exemple, les fils orthodontiques réduisent la fréquence des visites de suivi - et s'adapte bien aux structures anatomiques complexes, notamment en optimisant la flexibilité des endoprothèses cardiovasculaires. Par ailleurs, l'effet de mémoire de forme permet une implantation peu invasive et une déformation active des dispositifs médicaux. Par exemple, les attelles de fixation des fractures peuvent restaurer la contrainte de compression à la température du corps. Ces propriétés répondent directement aux problèmes cliniques, notamment le manque de rigidité, la complexité des procédures d'opération et la faible efficacité à long terme des dispositifs traditionnels.
À l'avenir, grâce aux avancées technologiques dans le domaine des SMA biodégradables (tels que les alliages de magnésium) et des dispositifs actifs (tels que les dispositifs de récupération à commande électrique), les SMA sont appelés à jouer un rôle plus révolutionnaire dans les dispositifs médicaux intelligents, les thérapies personnalisées et la chirurgie mini-invasive - par exemple, les échafaudages imprimés en 3D adaptés à la structure anatomique du patient et les implants intelligents qui peuvent réagir en temps réel aux signaux physiologiques. Ces avancées permettront à la médecine de passer de la "réparation passive" à la "régulation active", pour aboutir à un traitement plus sûr, plus efficace et plus personnalisé des maladies.
Lire aussi :
L'avenir, c'est maintenant : les alliages à mémoire de forme
Les alliages à mémoire de forme Ni-Ti et leurs constituants
Superélasticité et mémoire de forme du nitinol
Comment finaliser vos demandes pour le Nitinol
Expérience sur le fil de nitinol à mémoire de forme par SAM
Les 6 principales applications médicales du nitinol
Références
[1] Kinji. Sato, Hideaki. Goto, Nobuhisa. Tomita, THE SHAPE MEMORY HEAT TREATMENT AND ENVIRONMENTAL TEMPERATURE FOR IMPROVEMENT OF FORMING LIMIT ON TI-NI BASED SHAPE MEMORY ALLOY, Editor(s) : W.B. LEE, Advances in Engineering Plasticity and its Applications, Elsevier, 1993, Pages 1117-1125, ISBN 9780444899910, https://doi.org/10.1016/B978-0-444-89991-0.50153-0.
[2] N.B Morgan, Medical shape memory alloy applications-the market and its products, Materials Science and Engineering : A, Volume 378, Issues 1-2, 2004, Pages 16-23, ISSN 0921-5093, https://doi.org/10.1016/j.msea.2003.10.326.
[3] Tarniţă D, Tarniţă DN, Bîzdoacă N, Mîndrilă I, Vasilescu M. Propriétés et applications médicales des alliages à mémoire de forme. Rom J Morphol Embryol. 2009;50(1):15-21. PMID : 19221641.
[4] Ward B, Parry J. Routine intramédullary screw versus plate fixation of lateral mleolus fractures. Eur J Orthop Surg Traumatol. 2025 May 31;35(1):222. doi : 10.1007/s00590-025-04341-1. PMID : 40448862.
[5] Behrang Tavousi Tehrani, Shervin Shameli-Derakhshan, Hossein Jarrahi, An overview on Active Confinement of Concrete column and piers Using SMAs. Février 2017, https://www.researchgate.net/publication/310505502_An_overview_on_Active_Confinement_of_Concrete_column_and_piers_Using_SMAs

 Barres
Barres
 Perles et sphères
Perles et sphères
 Boulons et écrous
Boulons et écrous
 Creusets
Creusets
 Disques
Disques
 Fibres et tissus
Fibres et tissus
 Films
Films
 Flocon
Flocon
 Mousses
Mousses
 Feuille d'aluminium
Feuille d'aluminium
 Granulés
Granulés
 Nids d'abeilles
Nids d'abeilles
 Encre
Encre
 Stratifié
Stratifié
 Grumeaux
Grumeaux
 Mailles
Mailles
 Film métallisé
Film métallisé
 Assiette
Assiette
 Poudres
Poudres
 Tige
Tige
 Feuilles
Feuilles
 Cristaux simples
Cristaux simples
 Cible de pulvérisation
Cible de pulvérisation
 Tubes
Tubes
 Laveuse
Laveuse
 Fils
Fils
 Convertisseurs et calculatrices
Convertisseurs et calculatrices
 Écrire pour nous
Écrire pour nous
 Chin Trento
Chin Trento



